Services d’analyse omique
L’équipe d’expert·e·s de C3G en bio-informatique et en développement logiciel possède une vaste expérience dans l’analyse de données omiques complexes et leur transformation en découvertes significatives. Notre équipe maîtrise un large éventail d’analyses omiques et met à profit des méthodes computationnelles avancées.
Nos services comprennent :
Analyse de données personnalisée réalisée par des expert·e·s en bio-informatique
Développement de logiciels bio-informatiques sur mesure
Conception de bases de données et de portails pour l’organisation et le partage des données
Accompagnement à la conception expérimentale
Soutien à la préparation de demandes de subvention
Formation en bio-informatique offerte sur demande
Portefeuille
Expression génique unicellulaire
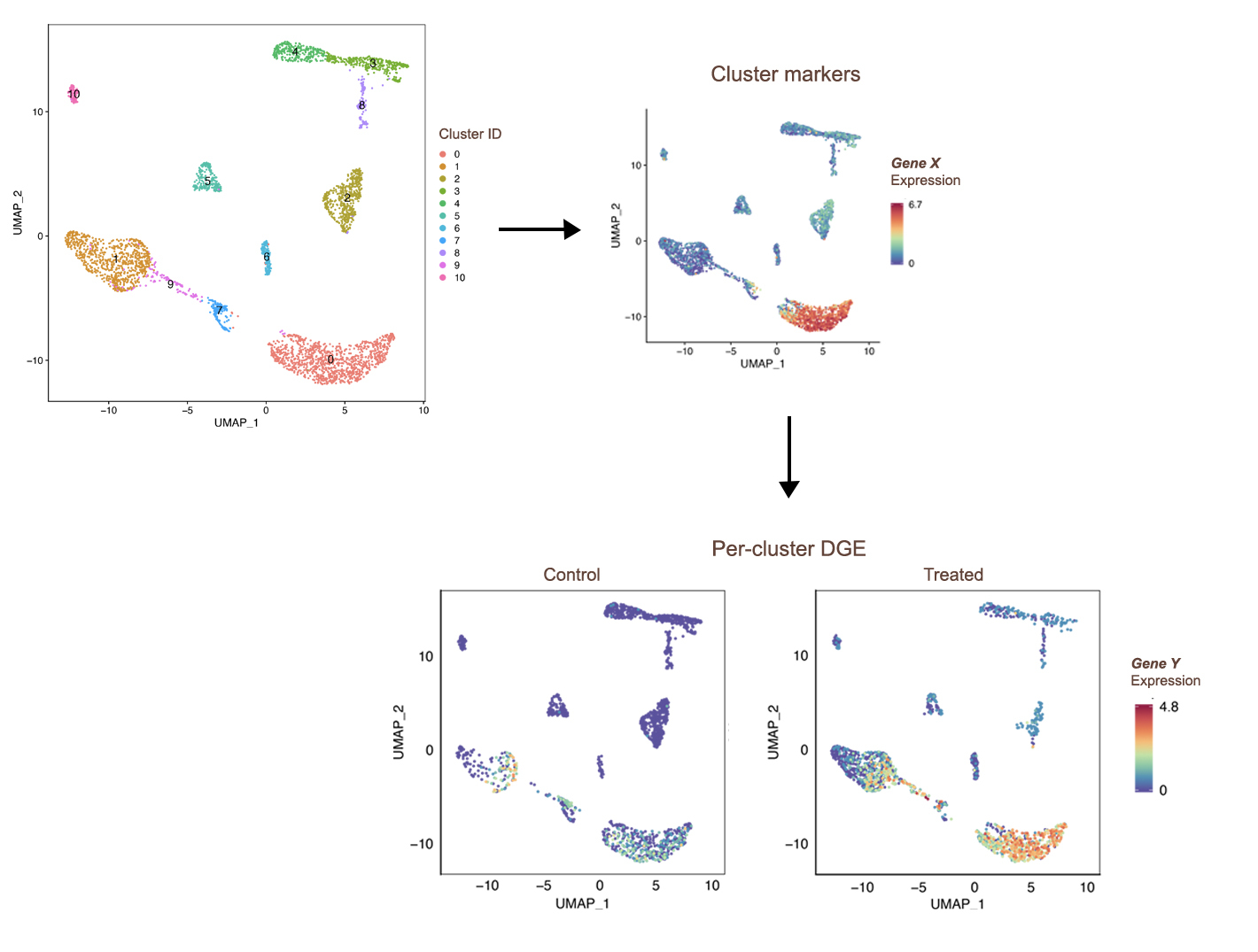
Le séquençage d’ARN unicellulaire (scRNA-seq) a considérablement élargi l’étude des systèmes biologiques complexes en permettant le profilage de l’expression à l’échelle du génome au niveau des cellules individuelles. Nous offrons des services complets d’analyse scRNA-seq, notamment :
- Traitement des données brutes : alignement et génération de matrices gènes-codes-barres avec Cell Ranger, alevin fry ou des outils équivalents.
- Contrôle de la qualité et filtrage : évaluation approfondie des indicateurs de qualité des cellules, notamment la détection des cellules de faible qualité, des doublets et de la contamination par l’ARN ambiant.
- Démultiplexage : Démultiplexage d’échantillons basé sur la génétique et les algorithmes à partir de bibliothèques de cellules individuelles groupées.
- Normalisation et correction : Normalisation des données, correction par lots, correction de l’ARN ambiant et autres étapes pour garantir une analyse en aval précise.
- Regroupement et identification des types cellulaires : Regroupement des cellules et annotation des types cellulaires sur la base de l’expression des gènes marqueurs.
- Exploration des données : Visualisation et exploration interactives des données.
- Expression génique et cartographie tissulaire : Reconstruction des processus cellulaires dynamiques tels que les voies de différenciation et les relations de lignée.
- Intégration multiomique : Intégration avec des types de données complémentaires, incluant l’ATAC‑seq sur noyaux uniques (snATAC-seq), le profilage immunitaire (p. ex. CITE-seq) et la transcriptomique spatiale.
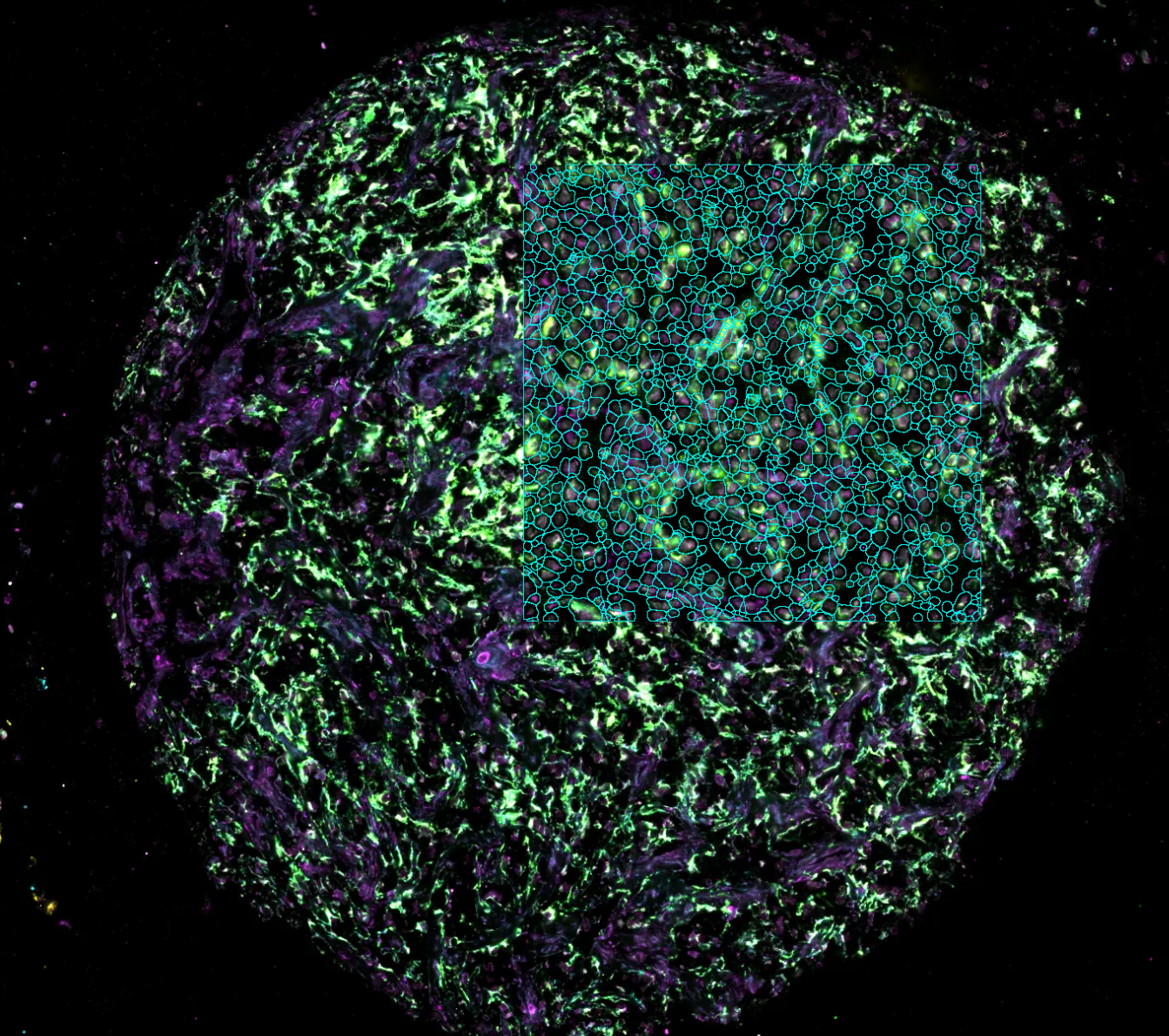
Transcriptomique spatiale
Cartographier l’expression génétique directement dans son contexte spatial original au sein d’un tissu. Depuis 2018, les publications en transcriptomique spatiale ont augmenté de façon exponentielle. Cette approche est largement utilisée en oncologie, neurosciences, immunologie et biologie du développement.
Nous offrons des services d’analyse complets pour diverses technologies, comme Visium ou GeoMx, incluant :
- Traitement des données brutes : Alignement et génération des matrices gène-code-barres.
- Traitement d’images : Segmentation cellulaire et identification des coordonnées des transcrits.
- Contrôle de qualité et filtrage : Évaluation rigoureuse des métriques de qualité, incluant la détection des cellules de faible qualité.
- Normalisation et correction : Normalisation des données, correction des effets de lot et correction de l’ARN ambiant, ainsi que d’autres étapes essentielles pour assurer la fiabilité des analyses ultérieures.
- Regroupement et identification des types cellulaires : Clustering des cellules et annotation basée sur l’expression des gènes marqueurs.
- Exploration des données : Outils de visualisation et d’exploration pour soutenir la génération d’hypothèses.
- Analyse différentielle de l’expression et de l’abondance : Identification des gènes et populations cellulaires présentant des variations d’expression ou d’abondance selon les conditions ou groupes.
- Cartographie tissulaire et de l’expression génétique : Reconstruction de processus cellulaires dynamiques, tels que les trajectoires de différenciation et les relations de lignée.
- Intégration multi-omique : Intégration avec d’autres types de données, incluant le snATAC-seq, le profilage immunitaire (p. ex. CITE-seq) et la transcriptomique spatiale.
RNA-Seq
L’un des services les plus fréquemment demandés, notre équipe peut vous aider à tirer le meilleur parti de vos données RNA‑seq. Ce service comprend généralement :
- Prétraitement : Alignement, assemblage et quantification de l’expression.
- Contrôle de qualité et filtrage : évaluation approfondie des indicateurs de qualité des échantillons, incluant la détection de gènes faiblement exprimés, l’analyse exploratoire des données (EDA), l’analyse en composantes principales (ACP ou PCA en anglais), etc.
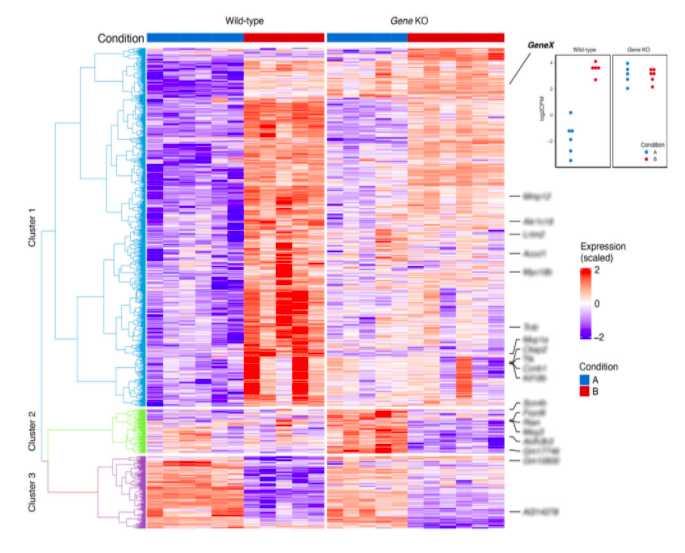
- Analyse différentielle et analyse de voies : Analyse en aval de l’abondance des transcrits, incluant l’expression différentielle, l’analyse Gene Ontology (GO) et l’enrichissement des voies KEGG.
- Visualisations personnalisées.
- Analyse des gènes et des voies : Analyse de l’expression par ensembles de gènes (GSEA), analyses d’ontologie des gènes (GO) et enrichissement de voies biologiques.
- Intégration multiomique : Intégration des données RNA‑seq avec d’autres types de données, notamment scRNA‑seq, ChIP‑seq, ATAC‑seq, etc.
- Autres analyses basées sur l’ARN : Analyse de l’épissage alternatif, détection d’eSNV, détection de fusions, déconvolution, PDX, décontamination, etc.
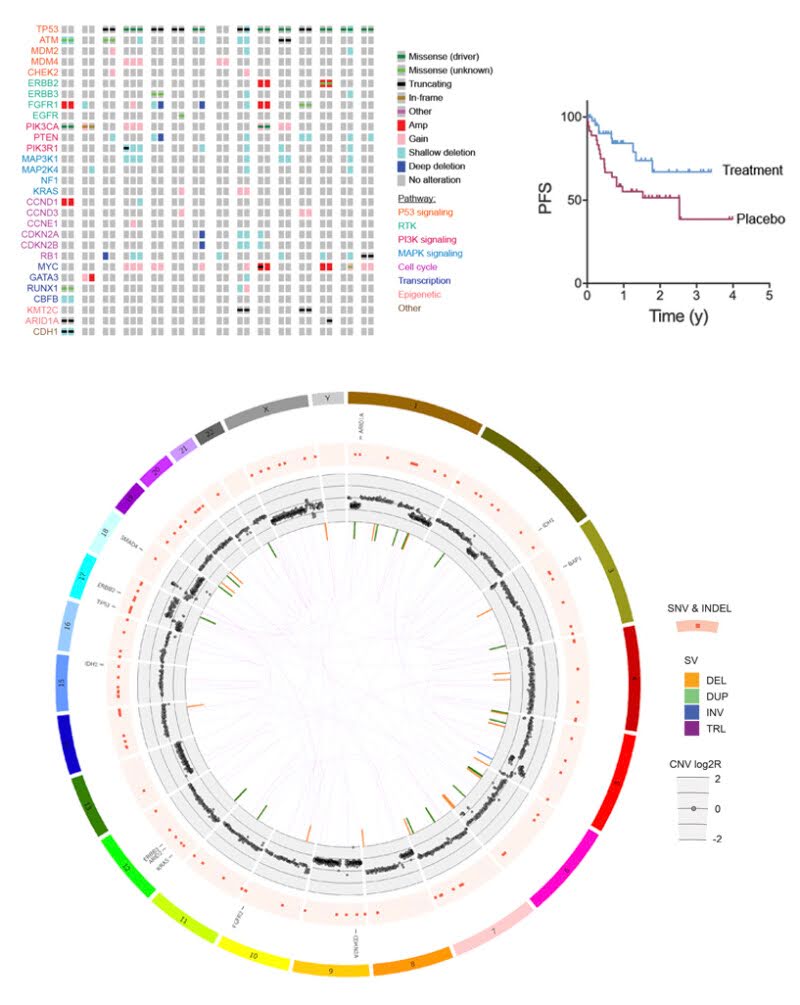
Génomique du cancer
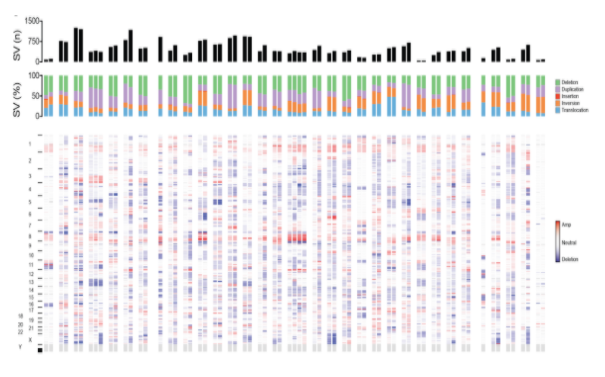
En séquençant l’ADN provenant à la fois d’un tissu tumoral et d’un échantillon normal apparié (sain), le séquençage génomique complet (whole‑genome sequencing, WGS) permet d’identifier de manière exhaustive de nouveaux variants associés au cancer. Nos services de bio-informatique en oncogénomique offrent une solution analytique complète de bout en bout, incluant :
- Détection de variants somatiques : Identification des SNV, indels, altérations du nombre de copies et variants structuraux somatiques grâce à une approche de type ensemble combinant plusieurs outils complémentaires.
- Annotation clinique et fonctionnelle : Intégration d’annotations pertinentes en oncologie à l’aide du Personal Cancer Genome Reporter (PCGR) et du Cancer Predisposition Sequencing Reporter (CPSR), fournissant des informations sur l’impact fonctionnel, la pertinence thérapeutique, la charge mutationnelle et l’instabilité des microsatellites (MSI).
- Analyse des variants structuraux : Utilisation de la suite GRIDSS–PURPLE–LINX pour une détection et une interprétation haute résolution des variants structuraux somatiques, combinant l’appel des SV, le profilage du nombre de copies et l’annotation des événements pour clarifier les réarrangements génomiques complexes.
- Contrôle de qualité et vérification de l’identité des échantillons : Pipeline rigoureux de contrôle de qualité et vérifications croisées de concordance des échantillons pour assurer l’intégrité des données.
- Intégration multiomique : Intégration des données RNA‑seq appariées afin d’identifier les variants exprimés et les fusions géniques, améliorant ainsi l’interprétation biologique et clinique.
- Soutien pour les modèles expérimentaux : Flux de travail adaptés aux xénogreffes dérivées de patient (PDX) et aux modèles tumoraux murins.
- Analyse accélérée pour les études prospectives : Options de traitement rapide pour soutenir les études cliniques et translationnelles prospectives.
Séquençage du génome entier (WGS) et séquençage de l’exome (WES)
Nous possédons une vaste expertise dans l’identification de variants à partir de données issues du séquençage du génome entier (WGS) ou du séquençage de l’exome (WES). Ce service comprend généralement :
- Traitement des données brutes : Traitement des données de séquençage jusqu’à l’appel des variants, conformément aux meilleures pratiques du GATK.
- Détection de variants structuraux et de CNV : Identification des variants structuraux et des variations du nombre de copies.
- Annotation et filtrage des variants : Annotation et filtrage adaptés aux besoins spécifiques du projet pour soutenir la priorisation des variants (p. ex. variants de novo, hétérozygotes composites dans des trios, à l’aide du cadre GEMINI/Slivar).
- Études d’association pangénomique (GWAS).
- Intégration multiomique.
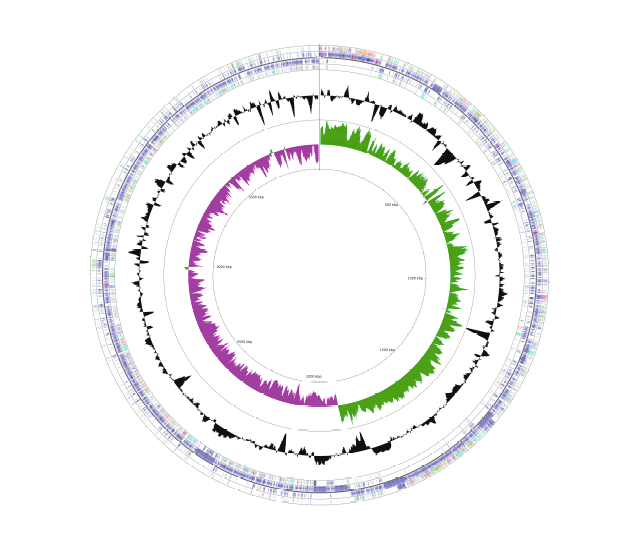
Assemblage et annotation du génome
Le séquençage à longues lectures (p. ex. PacBio HiFi, ONT) permet de capturer de grandes régions complexes du génome (p. ex. éléments transposables, séquences répétées, îlots d’ARNr) en une seule lecture longue, ce qui facilite leur ancrage précis dans un assemblage de novo. Nous possédons une vaste expertise dans l’assemblage de novo de génomes nouveaux, tant de petite taille (haploïdes : procaryotes, archées) que de grande taille (diploïdes : eucaryotes), en utilisant à la fois les technologies à longues lectures et les lectures courtes dans des approches hybrides. Notre boîte à outils comprend notamment :
- Assemblage et raffinement d’assemblages de novo à l’aide de données provenant de technologies complémentaires.
- Processus complets d’annotation, par exemple à l’aide de PGAP, BRAKER4, EGAPX.
- Détection, polissage et circularisation de chromosomes bactériens ou d’autres molécules circulaires (plasmides, mitochondries).
- Génomique comparative avec des assemblages existants, par exemple à l’aide d’OrthoFinder.
- Appel de variants basé sur une référence, incluant les indels, SNP, réarrangements structuraux importants et allèles phasés.
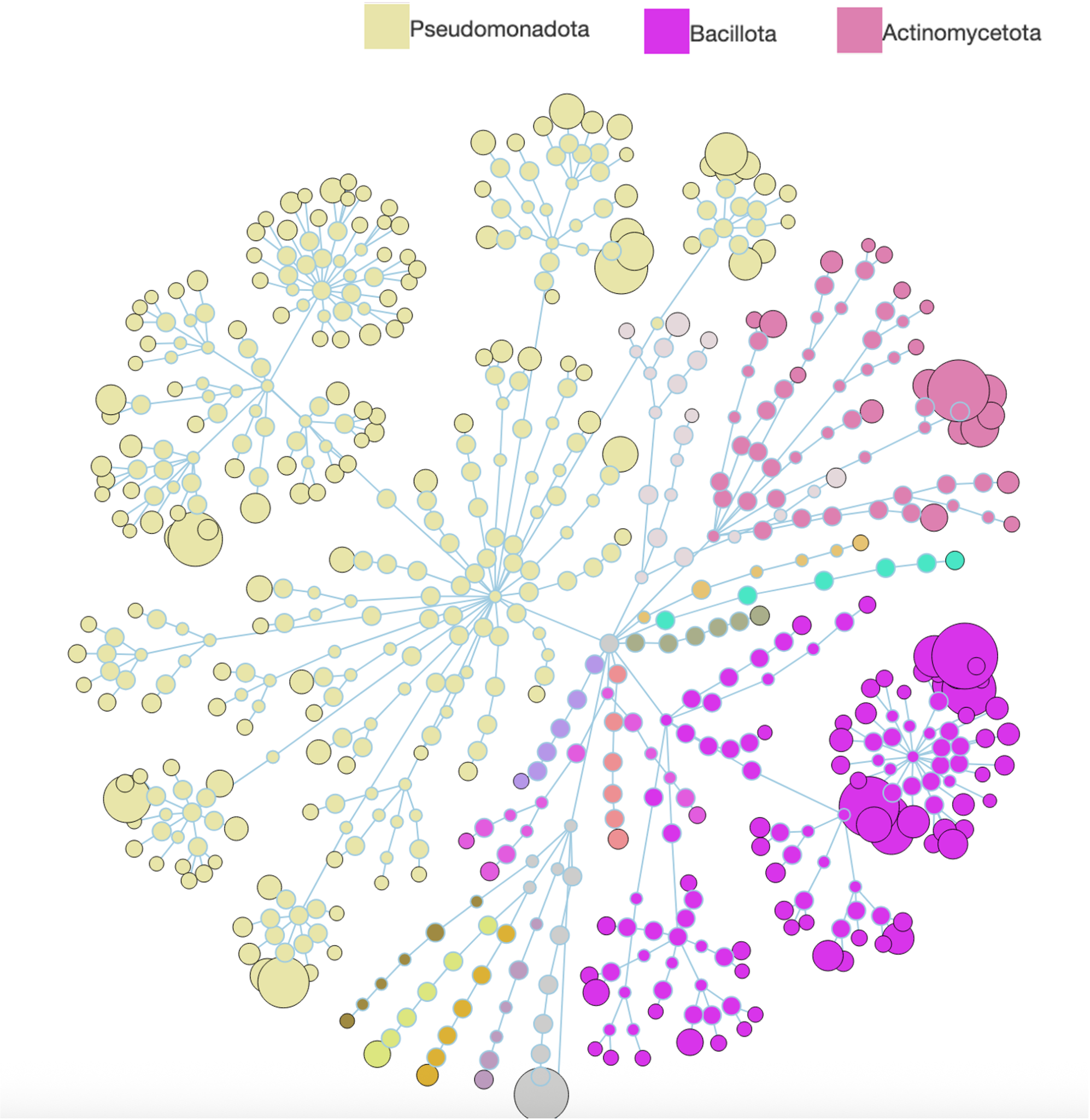
Microbiome et métagénomique
Nous nous engageons à offrir des services de pointe pour la recherche en métagénomique et en métatranscriptomique. Nos pipelines analytiques entièrement intégrés, à la fine pointe de la technologie, soutiennent une vaste gamme de conceptions expérimentales, notamment :
- Métagénomique basée sur amplicons (16S, 18S, ITS, COI)
- Métagénomique shotgun (WGS)
- Métatranscriptomique (RNA‑seq)
Nos analyses permettent d’obtenir des informations avancées, telles que les réseaux métaboliques globaux KEGG et les réseaux de co‑occurrence, générés à partir des données WGS et 16S à l’aide de la plateforme interactive MicrobiomeAnalyst.
Livrables clés pour la métagénomique basée sur des amplicons (16S, 18S, ITS, COI) :
- Dénoysement des lectures brutes en ASV à l’aide d’un flux de travail basé sur DADA2 ou QIIME
- Assignation taxonomique des ASV
- Annotation fonctionnelle de la communauté microbienne
- Fichiers de sortie entièrement compatibles avec MicrobiomeAnalyst et Calypso, permettant aux chercheur·euse·s de générer facilement des figures personnalisées prêtes pour la publication.
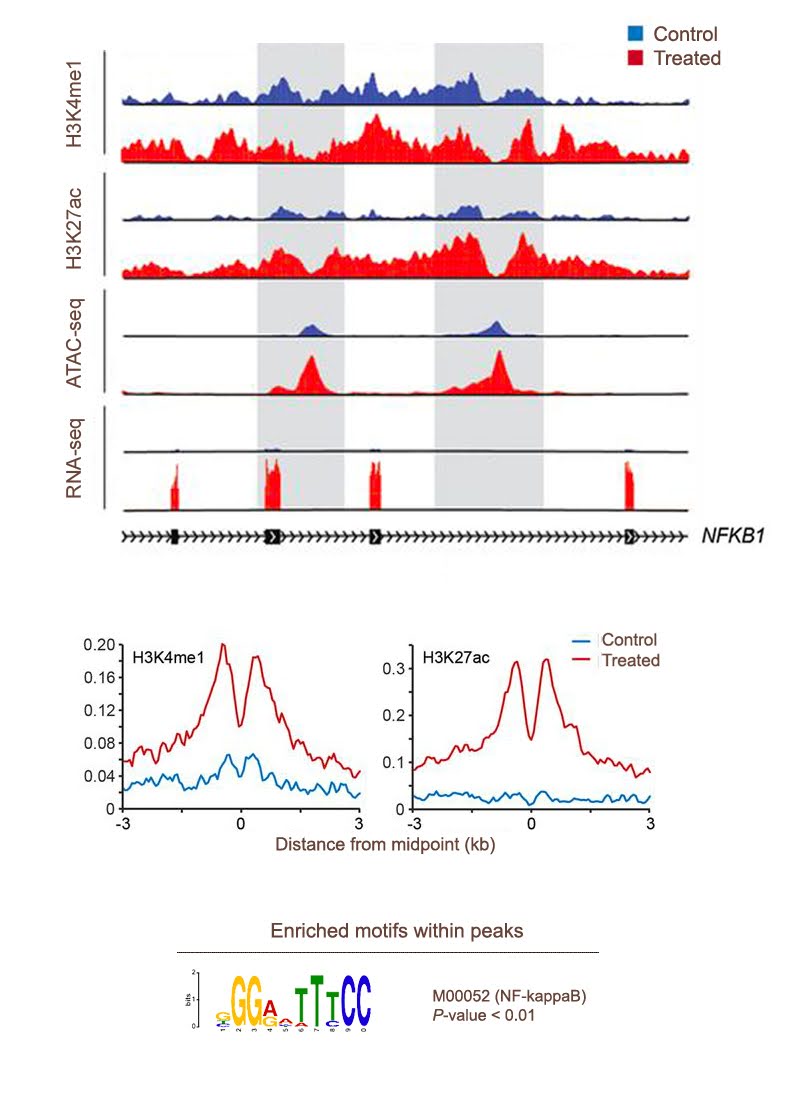
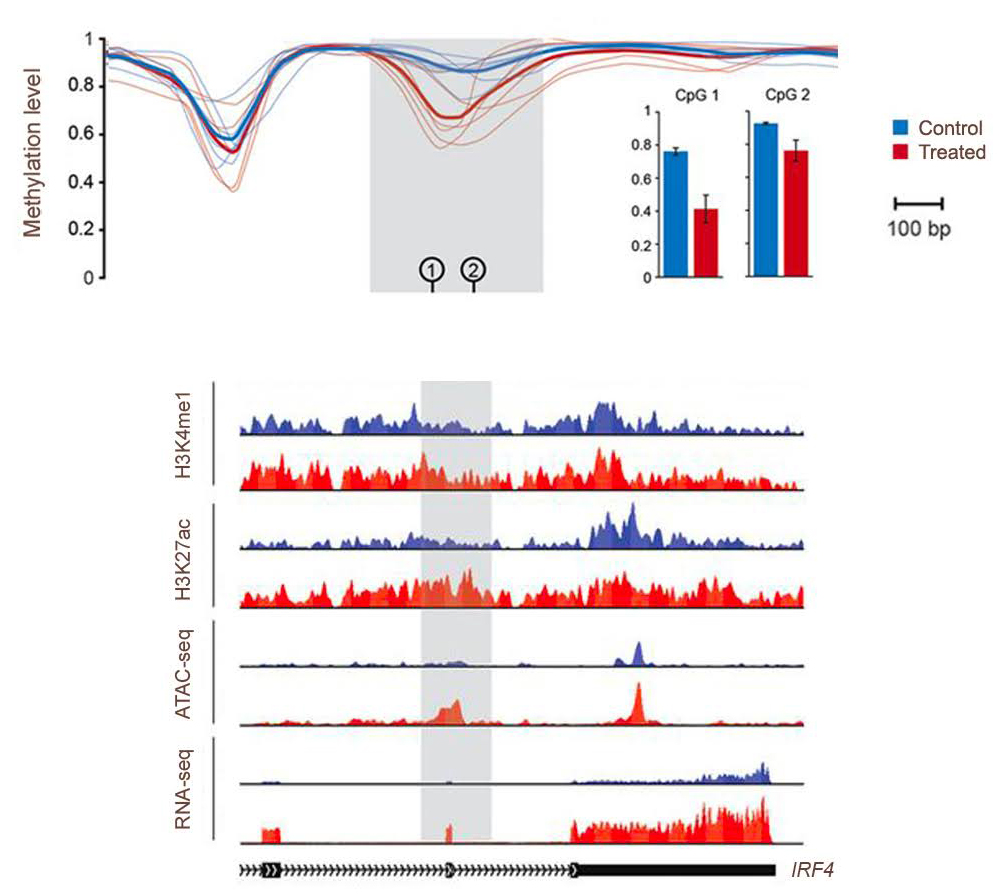
Bio-informatique épigénomique
Les profils génomiques à grande échelle des interactions ADN‑protéines, des modifications d’histones et des régions d’accessibilité de la chromatine fournissent des informations essentielles sur l’organisation du génome régulateur.
- Appel et annotation des pics : pour les analyses ChIP‑seq, ATAC‑seq et autres approches similaires (p. ex. CUT&RUN), nous produisons une liste de pics significatifs annotés selon leur contexte génomique ainsi que leurs enrichissements en motifs.
- Couverture génomique : pour le Methyl‑seq, nous effectuons l’alignement des lectures issues de la conversion bisulfite sur un génome de référence, suivi de la quantification des niveaux de méthylation.
- Interactions chromatiniennes à l’échelle du génome : pour le Hi‑C, nous construisons des matrices de contacts et générons des cartes de contacts multi‑résolution pour les analyses en aval, incluant l’identification et l’annotation des domaines d’association topologique (TADs).
- Visualisation personnalisée : nous générons des pistes épigénétiques via l’UCSC Genome Browser ou le WashU Epigenome Browser. Des graphiques métagènes et des cartes thermiques d’enrichissement sont également produits.
- Analyse différentielle : détection des pics (ou régions génomiques) présentant des variations de signal statistiquement significatives entre traitements ou conditions.
- Intégration multiomique : intégration avec d’autres types de données, incluant scRNA‑seq, RNA‑seq, ChIP‑seq, ATAC‑seq, Methyl‑seq, Hi‑C, etc.
Bio-informatique structurale
Nous pouvons vous accompagner en bioinformatique structurale, en complément d’autres analyses génomiques. Ce service comprend généralement :
- Visualisation de structures
- Cartographie des mutations
- Simulation dynamique moléculaire et calcul des énergies de liaison
- Cartes de contacts
Assemblage de novo du transcriptome (RNA‑seq)
Pour les organismes ne disposant pas d’un génome ou d’un transcriptome de référence de haute qualité, nos services d’assemblage de novo de données RNA‑seq permettent une caractérisation complète du transcriptome à l’aide d’approches à la fine pointe. Nos services comprennent :
- Assemblage et quantification du transcriptome : assemblage de novo des données RNA‑seq avec Trinity, suivi de l’estimation de l’abondance des transcrits et de l’évaluation de la qualité.
- Annotation fonctionnelle : annotation complète des transcrits à l’aide de Trinotate, incluant les recherches d’homologie, l’identification de domaines protéiques et la classification fonctionnelle.
- Analyse différentielle et analyse de voies : analyse en aval de l’abondance des transcrits, incluant l’expression différentielle, l’analyse d’ontologie des gènes (GO) et l’enrichissement des voies KEGG.
- Visualisation et rapports : production de visualisations et de rapports personnalisés pour faciliter l’interprétation et la communication des résultats.
- Intégration multiomique : intégration des données RNA‑seq avec d’autres types de données, incluant scRNA‑seq, ChIP‑seq, ATAC‑seq, etc.
Nous offrons un soutien flexible et adapté aux besoins spécifiques du projet pour un large éventail d’applications en recherche, allant de la biologie fondamentale à la génomique appliquée chez des organismes non modèles.
Autres – Omique
- Autres analyses unicellulaires (snATAC‑seq, snDNA‑seq)
- Microréseaux d’expression et de méthylation
- Analyses de séquençage diverses : DRIPc‑seq, RIP‑seq, etc.
- Séquençage de miARN et d’autres petits ARN
- Analyses de données CRISPR‑Cas9 et analyses statistiques associées
- Séquençage de pools (Pool‑seq)
- Génomique des populations : GBS, RAD‑seq
- CyTOF
- Intégration de données métabolomiques prétraitées
- Analyse de données protéomiques prétraitées
- Analyses intégratives — p. ex. Similarity Network Fusion (SNF)
- Visualisation et analyse de réseaux
- Analyse d’images
Témoignages